Candidatos vacunales cubanos: De los ensayos preclínicos a la inmunización

Hitos de Soberana
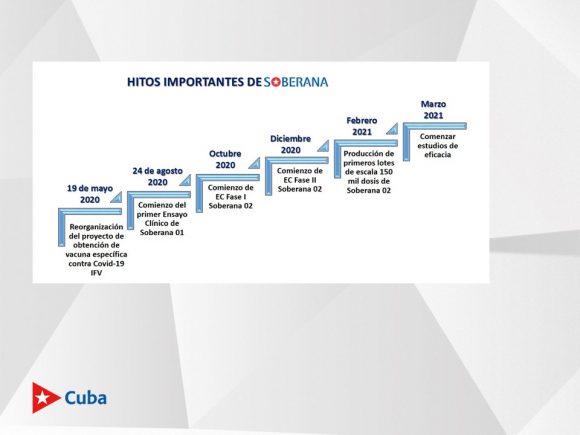
En un breve recorrido por el camino recorrido hasta hoy en el desarrollo de los proyectos cubanos de vacunas, Yury Valdés Balbín, director adjunto del Instituto Finlay de Vacunas, recordó que el punto de partida fue el 19 de mayo de 2020, en la reunión con el presidente Miguel Díaz-Canel, y poco después, en agosto, se anunciaba que América Latina tenía su primer candidato vacunal en fase clínica, con el inicio del primer ensayo clínico de Soberana 01, y en octubre sucedía lo mismo con Soberana 02.
Posteriormente, en diciembre, comenzó la fase II de Soberana 02, a partir de evidencias presentadas a la autoridad regulatoria nacional. En febrero pasado llegó otro hito, la producción a escala con dos lotes a escala de 150 000 dosis.
“Eso es necesario para seguir hacia fases más avanzadas de estudios clínicos. Contábamos con la tecnología y éramos capaces de obtener a una escala productiva elevada dosis para comenzar estudios de mayor envergadura.
“El 8 de marzo empezamos los estudios de eficacia, con el ensayo fase III. En la primera fase de Soberana 02 contamos con 40 voluntarios, en la segunda fueron 900, con dos sitios clínicos, y en la tercera escalamos a otro nivel de complejidad”, señaló.
¿Cómo marcha el ensayo fase III de Soberana 02?
El objetivo de un ensayo fase III −explicó− es evaluar la eficacia, la protección que brinda la vacuna frente a la enfermedad, así como la seguridad e inmunogenicidad. En el caso del candidato vacunal profiláctico FINLAY-FR-2, en un esquema de dos dosis (0-28) y en otro de dos dosis con una dosis de refuerzo (0-28-[56-84]) para la población de 19 a 80 años de edad.
“En el ensayo fase I siempre hablamos de seguridad, con un sitio clínico y un número reducido de sujetos, muy controlados. Se demuestra la seguridad y en el fase II la variable fundamental es la inmunogenicidad, empezamos a evaluar los elementos inmunológicos, y a partir de esos resultados podemos enfrentar el fase III, que es un estudio de eficacia”.
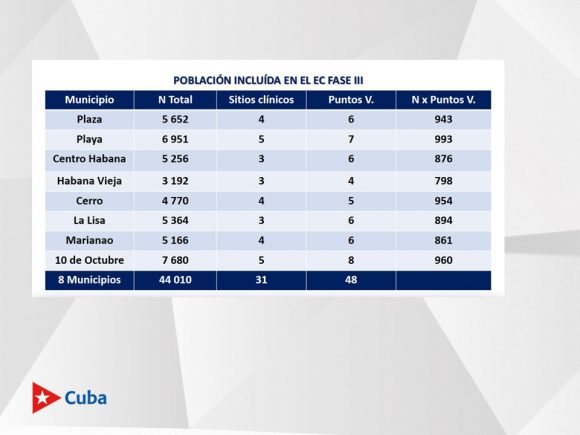
Al referirse a la muestra poblacional que participa en el ensayo fase III, en ocho municipios de La Habana, y respondiendo a una pregunta frecuente sobre por qué esos municipios, precisó que los estudios clínicos “tienen un diseño técnico en el cual participan muchos especialistas y nada se decide al azar. Estos eran los ocho municipios que, cuando se hizo el análisis, en el momento de presentar el protocolo, tenían la epidemiología más compleja y otros elementos que fueron evaluados.
“En aquel entonces hablábamos de que no íbamos a ser capaces de hacer un estudio de eficacia en Cuba, porque la cantidad de casos no alcanzaba para hacerlo. Y hubo que buscar alternativas en otros países. Es importante hacer este tipo de estudios en otras naciones para que las vacunas, con un desarrollo acelerado, se enfrenten a otras poblaciones”.
Sin embargo −añadió−, lo que ha sucedido luego en el país “nos ha dado la posibilidad de realizar el fase III en la capital. Lo que es negativo es número de casos, epidemiológicamente, ha sido un elemento importante en los ensayos”.
El fase III en ocho municipios ha incluido 44 010 sujetos (fueron 40 y 910 en los fase I y II), en 31 sitios clínicos (en comparación con uno en el fase I y dos en el fase II) y 48 puntos de vacunación.
“Cada uno de esos puntos de vacunación lleva un equipo de investigación, logística y toda una infraestructura. Un ensayo clínico de este tipo necesariamente incluye un mecanismo de gestión innovador. De esta magnitud, y en el contexto en que se realiza, no existen precedentes de ensayo clínico en Cuba.
“Una de nuestras capacidades ha sido prever las etapas. Desde que comenzamos el desarrollo clínico, sabíamos que este momento llegaría, y concebimos un sistema de gestión que nos permitiera manejar todos los ensayos clínicos en paralelo y con un mecanismo de gestión que nos permitiera hacerlos extensivos.
“Un ensayo clínico no es llegar, vacunarse y ya. Se llega tras la preparación de un grupo de condiciones, con un estándar regulatorio muy elevado”.
La organización, clave en el avance del ensayo
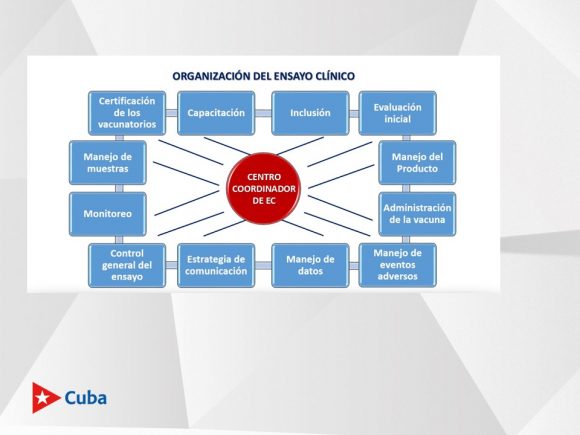
El centro coordinador de los ensayos clínicos mantiene estrechos vínculos con BioCubaFarma, el Minsap, la alta dirección del país, los Consejos de Defensa provinciales y municipales, con el fin de articular todas las decisiones que se toman alrededor de un ensayo clínico. “Es un proceso complejo, una gestión en tiempos de crisis que necesariamente demanda una lógica de organización”, apuntó el director adjunto del Instituto Finlay de Vacunas (IFV).
“En el ensayo clínico tenemos 12 procesos. Uno de ellos es la certificación de los vacunatorios, y son 48. Un vacunatorio no se parece al otro, tienen infraestructuras diferentes y están en localidades e instituciones distintas, pero todos tienen que cumplir un estándar.
“También hay procesos de capacitación, de inclusión; de manejo del producto, de distribución del producto a cargo de Encomed, que debe hacerlo con un estándar, manteniendo la cadena de frío y haciéndolo desde muy temprano. Además, de manera aleatorizada, porque este es un ensayo aleatorizado a doble ciega, todo está enmascarado: tuvo que haber un proceso de enmascaramiento del producto por actores que están fuera del ensayo. Realmente, gestionarlo lleva una alta complejidad”, dijo.
Otros procesos tienen que ver con la estrategia de comunicación dirigida a las comunidades, en la que se involucran activistas, líderes sociales y organizaciones de masas. Al ser aleatorizado el ensayo, los consultorios más cercanos al sitio de vacunación son los que entran, hay un grupo de componentes éticos y de rigor que se articulan.
“Hay que decir también que no todo siempre sale bien. No se puede decir que con los 44 010 sujetos todo ha sido excelente. Hay un proceso de mejora continua. Se van optimizando los procesos. Por ejemplo, el manejo de los casos es muy complejo en el ambiente de tensión.
“Y hay un seguimiento complejo. Cada uno de esos vacunados tiene una tarjeta que lo identifica para que siga un camino diferenciado, lo que genera complejidad y puede haber imprecisiones en el protocolo dentro del sistema de salud”.
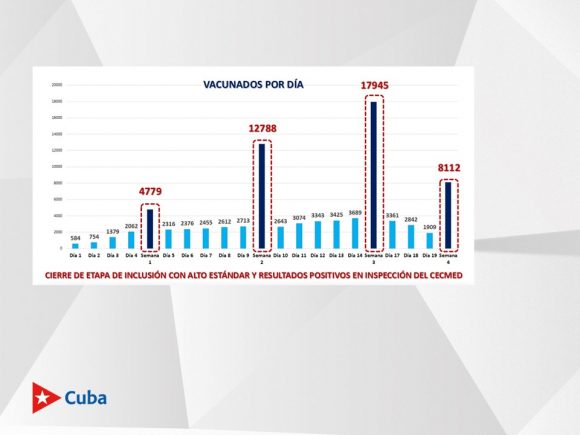
La primera semana fueron vacunados 4 779 sujetos; la segunda, 12 788, y la tercera, 17 945. “El mecanismo se fue engrasando. la estrategia comenzó con un sitio piloto en cada municipio el primer día, fuimos optimizando los procesos y ya el 10 de marzo fuimos incorporando más sitios al proceso. En solo 19 días logramos completar la muestra de 44 010 sujetos.
“Es importante que sepamos la dimensión de esto. Hay ensayos clínicos de las vacunas que hoy existen en el mundo que pasaron dos y tres meses para completar sus muestras. Y nuestra muestra ha sido superior en número. Nadie ha llegado a estos niveles. Tiene que ver también con la incidencia de la enfermedad, porque la nuestra es inferior, pero el tamaño de la muestra implica un reto logístico”, destacó el directivo del IFV.
“Como el esquema de nosotros es 0-28 y luego una dosis de refuerzo, el objetivo era en 28 días lograr poner todas las primeras dosis. Fue un esfuerzo muy grande para lograrlo en 19 días, con un alto estándar y con una inspección del Cecmed durante 10 días, que tampoco tiene precedente en la historia, con un sistema de inspecciones sorpresivas, sin avisar, todo aleatorio.
“El 31 de marzo, ayer, al cerrar el periodo de inclusión, tuvimos un pequeño contacto con cada uno de los sitios. Y fue una fiesta para cada sitio. El agradecimiento fundamental es a nuestro pueblo, porque se logran vacunar 44 010 sujetos en 19 días, porque existe una voluntad en el pueblo de acompañar lo que estamos haciendo por la vida”.
Sobre el sujeto número 44 010, vacunado este miércoles, dijo que se eligió el municipio Diez de Octubre porque tenía la mayor muestra de vacunación y en 15 de sus 18 días vacunó al 100% de los sujetos.
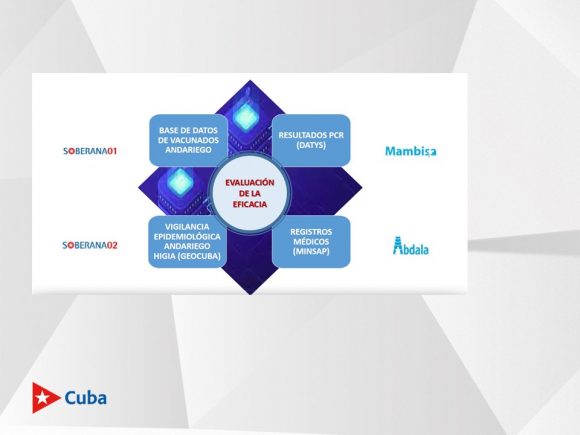
“Hay una diferencia en términos de evaluación. No es lo mismo manejar 900 que 44 010 sujetos. Hemos tenido que informatizar todo el estudio, uno de los elementos más complejos e innovadores que hemos tenido. Hoy Cuba cuenta con una base de datos de vacunados, desarrollada por GeoCuba.
“Pero con esa base de datos, por sí sola, tendríamos el inventario y no cómo evaluar la eficacia, el impacto en la enfermedad. La base de datos no lleva la enfermedad; entonces, tuvimos que articular esa base de datos de vacunados con los registros médicos del Minsap, que habla de la evolución, y los datos de todos los PCR. Las vacunas impactan en la enfermedad, pero también hay que evaluar cómo impactan en la transmisión. Usted puede no enfermar, pero estar infectado.
“Entonces, ¿cómo evaluamos la infección? Por los PCR. Hubo que anclar también la base de datos de los PCR, desarrollada por la empresa Datys. La interconexión entre esas tres bases de datos nos permiten hoy estar en una posición de evaluar las variables principales del ensayo. Y no solo con Soberana, sino con todos los candidatos vacunales cubanos”, apuntó
“Estos ensayos tienen que ser capaces de generar nuevas capacidades. Sin duda, nosotros seremos otros en capacidades de todo tipo cuando terminemos el desarrollo de nuestras vacunas”.
Explicó que cada día se realizan cierres de datos y cifras para continuar los procesos. “¿Por qué pudo Cuba hacer esto en 19 días? En primer lugar, por la integración de sus instituciones. No se trata de financiamiento, que sin dudas se están usando; no se trata de recursos. Se trata de valores y principios fundacionales y estructuras como el Minsap, BioCubaFarma y otras que trabajan juntas en función de la salud del pueblo. Es imposible hablar de cada una de estas instituciones, cuando lo que estamos haciendo es un esfuerzo de país.
“Segundo, por las capacidades creadas. Lo que nos ha diferenciado de otros lugares del mundo es que tenemos capacidades creadas. No se puede enfrentar la pandemia generando nuevas, tienen que existir. No sería posible sin el potencial humano, las ideas, el desarrollo farmacéutico, las capacidades productivas, los diseños de los ensayos por bioestadísticos y otras capacidades.
“En tercer lugar, había algo que le faltaba al ensayo clínico: el empuje que debe tener un ejercicio como este. Pensando en la sabiduría de Fidel, recurrimos a los jóvenes de tres universidades fundamentalmente: la de Ciencias Médicas, la Cujae, que hace hoy toda la captura de datos, y la Universidad de La Habana, que, además de formar parte del proyecto de Soberana 02, fue capaz de hacer algo que desde el Instituto Finlay no podíamos hacer, tener a alguien en cada sitio, porque nuestros trabajadores están en el desarrollo y producción de la vacuna.
“Cuando usted llega a un vacunatorio hoy, se encuentra no solo un potencial técnico y de salud de alto nivel, sino con los jóvenes con gran sentido de pertenencia que es capaz de movilizar y comprometer”.
Al concluir su intervención en la Mesa Redonda, el director adjunto del IFV hizo referencia a la canción de Buena Fe dedicada al candidato vacunal cubano.
“Apostamos por la educación, las capacidades y por el coraje. Nosotros somos consecuencia de nuestros antecesores, de la visión de Fidel y de nuestros fundadores. No hubiésemos podido hacer nada de esto si no hubiera sido también una voluntad política desde la máxima dirección del país hasta el último de nuestros trabajadores”.
Cenpalab y la importancia de los estudios preclínicos

Al intervenir en el espacio televisivo, Ileana Sosa Testé, directora de Toxicología Experimental en el Centro Nacional para la Producción de Animales de Laboratorio (Cenpalab), afirmó que es una fortaleza para Cuba contar con una institución científica de este tipo.
“Nuestro Comandante en Jefe avizoró la importancia de que existiera un centro como este, para el desarrollo de la industria médico-farmacéutica.
“Cenpalab tiene 132 hectáreas de extensión, muchos objetos de obra. Trabajamos con más de 13 especies de animales de laboratorio, más de 26 líneas de ratones, hámsteres, ratas, conejos, perros y primates de laboratorio. En los casi 40 años que cumple próximamente la institución, ha sido un reto para el país mantener los requerimientos y estándares regulatorios que tiene la producción de animales de laboratorio en el mundo”, dijo la especialista.
Al respecto, destacó que, del mismo modo en que se ha inspeccionado todo el sistema de producción de vacunas y ensayos clínicos, toda la parte preclínica (que precede a los ensayos clínicos en humanos) también es inspeccionada por los órganos reguladores de la sanidad animal, entre ellos el Centro Nacional de Sanidad Animal (Cenasa), por el Centro Nacional Coordinador de Ensayos Clínicos (Cencec) y el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (Cecmed).
“Todo tiene que estar protocolizado, escrito; tiene que haber un cumplimiento estricto de buenas prácticas no clínicas, porque de lo que se demuestre que va a pasar a humano tiene que quedar toda la data primaria registrada, donde se demuestre que ese proceso es de esa manera.
“En tiempos de pandemia, la situación de emergencia permite hacer ensayos en animales prácticamente en paralelo; es decir, se avanza con la investigación en las fases de eficacia, inmunogenicidad, y llegamos a la fase de la toxicología. Cenpalab es el encargado de hacer la toxicología terminal, la que va prácticamente a registro sanitario, de los productos más importantes que tiene no solo BioCubaFarma, sino el país, para uso humano, veterinario o que van a ser aplicados en la agricultura”, explicó.
Sobre este punto, destacó que es un potencial creado y capacidades que se han potenciado a partir de este tipo de emergencia que ha surgido y añadió que “tenemos diseñado dónde montar un ensayo con todas las necesidades cubiertas en cuanto al cumplimiento de las buenas prácticas no clínicas, sirviendo a todo el polo científico cubano en lo que implica necesidades de animales de laboratorio”.
La especialista explicó que son varias las tareas del centro en la Dirección de Toxicología y Experimentación animal, especializada en servicios de:
- Toxicología regulatoria BPL no clínica, para productos de uso humano
- Farmacología preclínica para productos de uso humano
- Toxicología regulatoria de productos de uso agrícola y medioambientales
- Ensayos clínicos fases I, II y III para vacunas veterinarias
- Servicios especializados de los laboratorios de química analítica, patología y clínica
“Vamos acompañando en todas las fases del desarrollo de un producto. El desarrollo de un producto es desde dos a 12 años, incluso 15, y durante todo este tiempo acompañamos. En tiempo de pandemia hay otro ritmo, es una emergencia. No solo realizamos los estudios que nos solicitan, sino que colaboramos con otras instituciones. Participamos interrelacionadamente con los desarrolladores de procesos experimentales para cubrir algunos aspectos a los cuales no pueden llegar debido al gran número de ensayos montados”, precisó.
Aseguró que todos los bioterios del Cenpalab están revisados por las autoridades regulatorias. “Desarrollamos la toxicología preclínica en BioCubaFarma, y cumplimos con protocolos y procedimientos establecidos y estandarizados, que además son constantemente auditados.
“En el caso de Cenpalab, la toxicología que hacemos es de tercera parte, una fortaleza adicional, porque no estamos vinculados directamente a ningún producto final. No somos productores, sino que damos este servicio: recibimos el producto y evaluamos si es o no seguro, si es o no tóxico, si tiene o no tiene eficacia”.
La directora de Toxicología Experimental del Cenpalab aclaró que en ninguno de los casos de desarrollo de vacunas, estas se prueban directamente en primates.
“Para llegar a estos, tiene que haber necesariamente un paso anterior. Por ejemplo en el caso de las vacunas que se están probando, se están utilizando hámsteres, ratones Balb/c, y en este caso la toxicología aguda se hace en ratas de laboratorio. Luego se vuelve a hacer la dosis repetida, con un alto nivel de volumen a suministrar, y luego es que se escala al primate como segunda especie. Son regulaciones establecidas por la OMS. Aunque las vacunas sean emergentes, hay que cumplir con todos los pasos.
“Es importante que todos los procesos transcurran a la par. En la mayoría de los casos, cuando ya se avanzó un poco en la clínica, se regresa atrás a revisar la data preclínica. De ahí que sea esencial que los datos de la preclínica estén disponibles y con la calidad requerida, porque los investigadores clínicos van necesitando en medio del proceso demostrar elementos que no se pueden demostrar en el humano y que implican ir necesariamente al modelo animal.
“Hemos trabajado todos los candidatos vacunales cubanos contra la COVID-19. En estos momentos, tenemos todo montado en primates y va a un buen ritmo. Para el mes de mayo debemos terminar toda la vacunación, que se realiza muy por encima de lo que se está haciendo en el humano. De este modo, terminamos los ensayos en primates. En el resto de los modelos animales, se ha cumplido todo lo establecido y las hipótesis que previeron nuestros científicos. Los ensayos van muy bien”.
Destacó que se han garantizado todos los modelos animales necesarios, “y este es un elemento fundamental porque a veces se necesitan muchos animales para montar varios estudios simultáneos. Cenpalab ha dado una respuesta importante. Tenemos una colonia de cuatro especies de primates, y el equipo de trabajadores que atiende a los primates del centro, si bien es pequeño, se ha crecido en estas circunstancias, apoyando todo el tiempo la investigación.
“Ha sido un reto para nosotros, para los equipos del CIGB, del Finlay, poder montar estos ensayos en primates. En medio de todos, estábamos terminando estudios con el Surfacén, montando estudios de Jusvinza, Nasalferón, el Itolizumab. Todos estos estudios al mismo tiempo implican un desafío, con estudios crónicos que llevan más de seis meses y más de 270 animales. Hemos abierto muchas capacidades, y podemos continuar ampliando las capacidades de ensayo”.
La directora de Toxicología Experimental del Cenpalab reconoció al equipo de 32 especialistas, con técnicos altamente especializados que han trabajado sin descanso durante este año de pandemia. “Creemos que el esfuerzo ha valido la pena, por toda la alegría que tenemos por el desarrollo de nuestras vacunas”, concluyó.




Deja una respuesta