BioCubaFarma e Instituto Finlay informan sobre inicio del ensayo clínico fase III del candidato vacunal Soberana 02
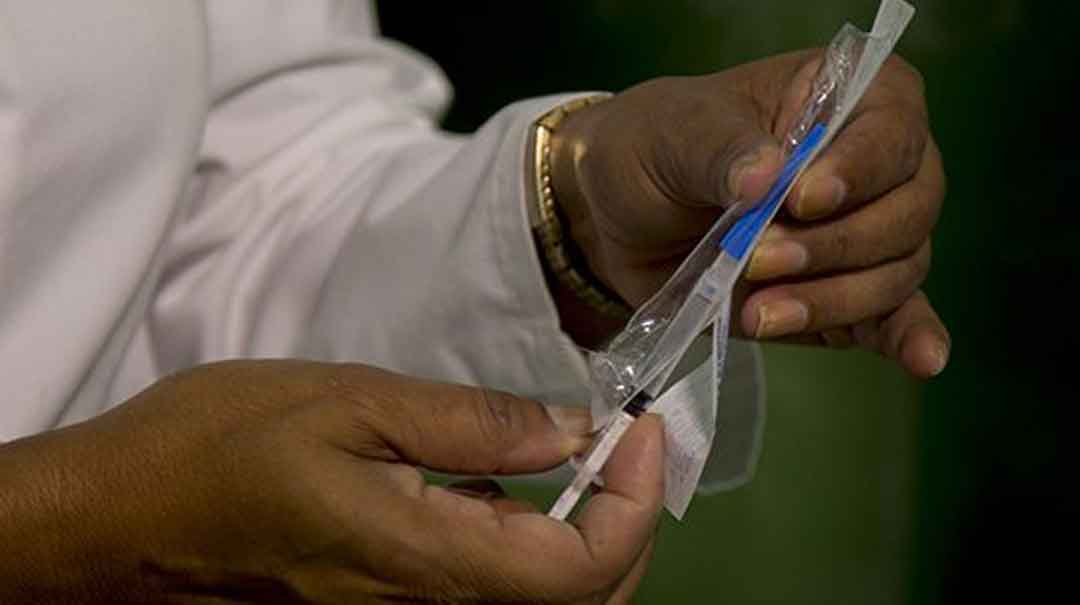
A partir de los datos obtenidos en la preclínica y los obtenidos sobre seguridad clínica en los estudios fase I y fase II, así como los resultados preliminares de inmunogenicidad recogidos en los ensayos clínicos fase I y fase II a, y considerando la necesidad de avanzar hacia otras fases de desarrollo del producto, se presentó al Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (Cecmed) el expediente solicitando la realización de un ensayo clínico fase III del candidato vacunal Soberana 02.
Ese ensayo fue aprobado este miércoles 3 de marzo de 2021, se precisó en la rueda de prensa.
“En esta gran batalla a nivel mundial por vencer a la pandemia, las vacunas han tenido grandes hitos y uno de ellos es cuando se les autoriza a pasar a un ensayo de fase III, porque ello quiere decir que la información que se va conformando va permitiendo pensar que las vacunas van a ser eficaces”, apuntó Vicente Vérez Bencomo, Director General del Instituto Finlay de Vacunas (IFV).

Dr. Vicente Vérez Bencomo, director general del Instituto Finlay de Vacunas. Foto: Irene Pérez/ Cubadebate.
De acuerdo con el experto, la vacuna Soberana 02 ha tenido un desarrollo farmacéutico, y preclínico, donde demostró en animales su seguridad y la inducción de la respuesta inmune. “Posteriormente inició un ensayo clínico Fase I, en el cual confirmó en primer lugar la seguridad en seres humanos y confirmó además cuál era la mejor opción en esquemas y de fórmula, para inducir una respuesta inmune potente y neutralizante del virus. Luego, la vacuna inició una Fase II dividida en dos etapas: una Fase IIa con 100 voluntarios, y una Fase IIb en la cual se incluyeron 810 voluntarios adicionales, para un total de 910 voluntarios.
“En este momento la Fase IIa está muy avanzada, y es a partir de las conclusiones preliminares que sostenemos que, los resultados de respuesta inmune de la Fase IIa y los de seguridad de la Fase IIb nos permiten iniciar la Fase III. Es la práctica que se ha seguido en la mayor parte de las vacunas en el mundo, donde se solapan un poco las etapas, porque de lo contrario este proceso demoraría 15 años”, dijo Vérez Bencomo.
Este ensayo Fase III, precisó, es el primero de los ensayos de eficacia, pues en los ensayos anteriores se demuestra respuesta inmune. “Pudiera pensarse que va a proteger a la persona, pero esa respuesta inmune tiene que demostrar que, efectivamente, la protege. Por lo tanto hay que constatar la eficacia, y esto se hace en vacunados y no vacunados, y en vacunados con placebo. Hay que demostrar que se enferman los que no se vacunan y los vacunados no se enferman. Y eso es parte de la etapa crucial de una vacuna”, refirió.
En el mundo de las vacunas contra la COVID-19, cómo se posiciona Soberana

Producción de nuevos lotes de Soberana 02. Foto: Alejandro Azcuy/ Cubadebate.
La Organización Mundial de la Salud reconoce hoy que existen 76 candidatos vacunales en alguna de sus fases de ensayo clínico, y 187 propuestas de candidatos vacunales que están en fase preclínica, explicó Dagmar García Rivero, directora de Investigaciones del Instituto Finlay de Vacunas (IFV).
De esas 76 vacunas en fase clínica, 24 son vacunas de subunidades, que es la plataforma de vacunas en la cual se clasifica Soberana y el resto de las vacunas cubanas. Por tanto, Soberana está entrando en una selecta lista de candidatos vacunales que han pasado a Fase III, que en total contabilizan 16, dijo.
De las 24 que hay de subunidades esta es la primera vacuna cubana y latinoamericana que avanza a Fase III y es un hito y un orgullo para la ciencia cubana, sostuvo.
Principales características del ensayo Fase III
Puntualizó el director general del IFV que el ensayo comenzará en 8 municipios de la capital cubana desde este jueves 4 de marzo: Plaza, Playa, 10 de Octubre, Centro Habana, Marianao, Habana Vieja, Cerro y La Lisa.
Se trata de un ensayo fase III multicéntrico, adaptativo y en grupos paralelos, aleatorizado, controlado con placebo y a doble ciego, en voluntarios de edades comprendidas entre 19 y 80 años, sin historia conocida de infección por SARS-CoV-2.
Tomando en consideración el incremento de la tasa de infección autóctona en la población total cubana, el acumulado de y, de manera específica, el incremento significativo durante enero-febrero de 2021 en la tasa de incidencia en la población de La Habana y el grupo etario de mayores de 19 años, se justifica la realización de un estudio fase III para evaluar la eficacia.
Lic. Yury Valdés Balbín, director adjunto del Instituto Finlay de Vacunas. Foto: Irene Pérez/ Cubadebate.
De acuerdo con Yury Valdés Balbín, director adjunto del IFV, el ensayo está concebido en tres grupos: un grupo placebo, un grupo que va a ser sometido a dos dosis del candidato vacunal Ssoberana 02, y un tercer grupo que va a tener un esquema de dos dosis de Soberana 02 con un combinado de una dosis de Soberana 01.
Sobre el tiempo de duración del mismo, el experto señaló que al igual que los ensayos que se han hecho en el mundo, este va a tener análisis interinos. “Son análisis que se van haciendo por test parciales de ensayo, y a partir de que uno cumpla la eficacia de la vacuna, los resultados parciales de estos ensayos pueden ser utilizados para avanzar en otras categorías como el autorizo de uso de emergencia. Eso es lo que ha hecho todo el mundo, y lo que nosotros tenemos concebido en nuestro estudio”.
No obstante, dijo, el estudio sí continúa, y tiene un tiempo de duración aproximadamente de tres meses, a partir de que se ponga la última dosis del tercer grupo. “Pero repito, se van haciendo análisis interinos. En la medida en que vayan apareciendo casos, hay determinados cortes. Si aparece un número determinado de casos, se puede hacer un análisis interino, que lo hace, a partir del manejo de la ética y del complimiento de todas las normas establecidas, un comité independiente. Ese análisis puede dar suficientes resultados como para seguir avanzando en otras modalidades del uso de la vacuna. De ahí que, el tiempo específico de duración de un ensayo no es exacto, depende de cómo se vaya desarrollando. También dependerá de la manera en que nosotros logremos incluir la muestra”, comentó.
Al respecto, aclaró que el ensayo se realizará en 44 010 voluntarios en un esquema de dos dosis y en otro de dos dosis con una dosis de refuerzo.
Los eventos adversos serán evaluados durante una hora de observación posterior a cada dosis en el sitio clínico y seguidamente se realizará vigilancia activa y pasiva con seguimiento ambulatorio hasta completar los 28 días después de aplicada cada dosis.
Agregó la doctora María Eugenia Toledo Romaní, investigadora principal del ensayo clínico fase III, del IPK, que “los voluntarios van a tener también un seguimiento especializado, con un protocolo estandarizado que ha sido avalado por el grupo de expertos nacional que sigue el estudio. Esto es mientras dure la administración de las diferentes dosis. Una vez terminada la administración de cada uno de los esquemas, los sujetos van a ser seguidos durante tres meses, de manera tal que se pueda vigilar si apareciera la enfermedad y así poder hacer la evaluación. Después de esos tres meses el grupo que recibió placebo va a recibir un esquema completo de vacunación, pues esto constituye un principio ético de la investigación”.
Los sujetos, después de haber recibido toda la información relativa al ensayo y de contar con un tiempo prudencial para el análisis de la información recibida, decidirán su participación en el estudio y firmarán el registro de formulación de consentimiento informado.
La selección de los sujetos será realizada por los investigadores clínicos designados al efecto, liderados por el investigador principal del estudio.
¿Cuáles son los criterios de inclusión de voluntarios?

Dra. María E. Toledo Romaní, investigador principal del ensayo clínico fase III, Instituto de Medicina Tropical “Pedro Kourí”. Foto: Irene Pérez/ Cubadebate.
Sobre los criterios de inclusión de los sujetos en el ensayo clínico, María Eugenia Toledo Romaní, investigadora principal del ensayo clínico fase III, del Instituto de Medicina Tropical Pedro Kourí, se ha tratado de concebir un ensayo de fase III que se parezca lo más posible a la realidad de nuestras poblaciones y que sean beneficiados lo más posible aquellos grupos que tienen un elevado riesgo de adquirir la infección, e incluso de poderla dispersarla y enfermar a los más vulnerables.
De acuerdo con la especialista, se ha concebido un ensayo clínico en una población entre 19 y 80 años, y el primer criterio de inclusión es que los voluntarios den su consentimiento informado, lo que representa los aspectos éticos a considerar en este tipo de investigación de eficacia, la cual busca demostrar que el candidato vacunal cubano es capaz de prevenir la enfermedad sintomática por SARS-CoV-2.
El otro criterio de inclusión es que se consideren mujeres en edad fértil pero que no estén embarazadas y estén dispuestas a no embarazarse durante el tiempo que dure el estudio, para poder seguir en él, pues no se ha probado todavía la seguridad en poblaciones como las gestantes.
“Hay un grupo de criterios en cuanto a cómo se va a seleccionar esa población: se va a estratificar entre los mayores o iguales a 65 años y hasta 80 años, la población menor de 65 años sin riesgo de complicaciones y la población menor de 65 años con riesgo de complicaciones. Hoy sabemos por la literatura internacional y por la casuística cubana que hay población con elevado riesgo de complicaciones, en esto influye por ejemplo la obesidad, las enfermedades crónicas descompensadas, que han sido las principales causas que han aportado a la mortalidad pos SARS-CoV-2”, precisó Toledo Romaní .
Entre los criterios de exclusión del estudio están que el sujeto haya tenido una enfermedad febril o infecciosa aguda en los siete días previos a la administración de la vacuna o en el momento de su aplicación; historia previa o actual de infección por SARS-CoV-2, o la aplicación de vacunas que contengan anatoxina tetánica en los últimos tres meses.
Además, mujeres que estén embarazadas, puerperio o lactancia, así como personas con enfermedades descompensadas que limiten la vacunación según criterio clínico.
“Hay otros criterios de exclusión como es el uso de inmunomoduladores, inmunosupresores o inmunoestimulantes. Sabemos que hay pacientes con enfermedades crónicas que usan este tipo de medicamentos, pero también se ha usado en la población Nasalferón y otros medicamentos que tienen efecto inmunomodulador. Entonces si estos medicamentos han sido utilizados en los últimos 30 días por los sujetos no van a quedar incluidos en el estudio”, dijo.
¿Cómo está organizado el ensayo fase III desde la atención primaria de salud?

Dra. Mayra García Carmenate, investigadora coordinadora a nivel provincial del ensayo clínico fase III, MINSAP. Foto: Irene Pérez/ Cubadebate.
De acuerdo con la doctora Mayra García Carmenate, investigadora coordinadora a nivel provincial del ensayo clínico fase III, para esta etapa fueron ocho los municipios de la capital involucrados en la Fase III, en los cuales se implementará a nivel de policlínicos una estrategia de aleatorización de la población.
“Eso nos va a permitir tener la selección de unos primeros consultorios, posteriormente otros y más tarde poder llegar a todos los consultorios que tiene ese policlínico. Ahí, cumpliendo los criterios de inclusión y exclusión, se va a estar evaluando a la población que tiene entre 19 y 80 años, que cumplan con estos criterios”, dijo.
Aclaró lo experta que “no significa que sea solo esa población. Todas las personas que tengan la voluntad de participar en el estudio, que pertenezcan a estos municipios, se van a dirigir a sus consultorios del médico de la familia o al policlínico que le corresponde y allí se le darán todas las orientaciones para que pueda dirigirse al médico que va a estar evaluando a cada uno de los sujetos, y poder determinar si puede ser o no incluido en el estudio”.
Los ocho municipios de la capital incluidos en la Fase III son: Plaza de la Revolución, Playa, Diez de Octubre, Centro Habana, Marianao, Habana Vieja, Cerro y La Lisa, “los cuales fueron seleccionados por la situación epidemiológica que presentan hoy, de la incidencia de casos, a partir de lo que tenemos que demostrar, que es la eficacia de este candidato vacunal en la enfermedad”, dijo.
Tener una tasa elevada de contagios nos permitirá hacer esta evaluación, acotó la especialista.
“Este trabajo no comienza hoy. Ya con los consultorios seleccionados y los sitios clínicos, se ha ido haciendo un trabajo previo, identificando los potenciales de los posibles voluntarios a ser incluidos en el estudio. Porque esta es la primera etapa antes de solicitarle a las personas su consentimiento informado. Después, estas personas deben acudir a su consultorio, según orientaciones del médico de la familia para hacer la evaluación inicial”, apuntó por su parte María Eugenia Toledo Romaní, investigadora principal del ensayo clínico fase III, del Instituto de Medicina Tropical Pedro Kourí.
Según la experta, “se están usando todas las redes que existen en la comunidad, como está previsto en el sistema de atención primaria del país, para poder contactar a esas personas que ya fueron seleccionadas y pueden ser potenciales voluntarios, brindarles toda la información que necesitarían, poder responder todas las preguntas, explicarles cuáles son los beneficios y los riesgos, e incluso cómo resultarían beneficiados a los que se les administre el producto placebo, una vez culminada la etapa de seguimiento.
Una vez aclarada todas las dudas se hace el examen y el médico determina que cumple o no los criterios y puede participar en el ensayo”, dijo Toledo Romaní.
¿Qué elementos permiten medir la eficacia de la vacuna?

Ensayo clínico del candidato vacunal cubano Soberana 02. Foto: Abel Padrón Padilla/Cubadebate.
¿Con la actual tasa de incidencia de la COVID-19 en la capital, qué número de participantes en el ensayo tendría que contagiarse para establecer resultados concluyentes sobre la eficacia de la vacuna?
Al respecto, Vicente Vérez Bencomo, director general del Instituto Finlay de Vacunas (IFV), explicó que en el diseño concebido de fase III y los análisis estadísticos hechos, el primer corte sería cuando aparecieran 53 enfermos.
“Es importante aclarar que todas las vacunas preventivas contra la COVID-19 lo primero que miden es enfermo, no cero positivo, pues son positivos a PCR. Es decir, 53 enfermos son 53 personas que se clasifican de este modo. Todas las enfermedades infecciosas, en este caso la infección por COVID-19, tienen dos fases: una primera es la de infección, en la cual el virus se queda en las vías superiores, y se tiene PCR positivo. Pero, hay muchas personas que evolucionan asintomáticamente, o sea que no se enferman, transmiten el virus, pero no tienen síntomas”, comentó.
Refirió el experto que lo que miden las vacunas, cuando se habla de un 90 y tanto de eficacia, es la eficacia en prevenir la enfermedad, la cual se define a partir de la aparición de síntomas. ¿Eso cómo se mide? “La muestra total es de 159 casos al final del ensayo. Cuando aparezcan los primeros 53, se hace un corte y se evalúa. Si su vacuna es muy buena y los 53 aparecen en el placebo, ahí mismo usted puede detener el ensayo y decir que la vacuna es 100 % eficaz”, detalló.
“Si en ese primer corte hay una relación de placebo contra vacuna con la cual 53 no es suficiente, hay que seguir, hasta que aparezcan 106, y ahí se hace un segundo corte. Y luego hasta que aparezcan 159. Esos son los tres momentos decisivos del estudio. Nosotros estamos diseñando otros estudios de eficacia y hay otras formas de evaluar la eficacia y la efectividad de una vacuna. Ahora preferimos concentrarnos en la fase III convencional y cuando avancemos un poco más hacia la autorización de estos otros ensayos, explicaremos de qué se trata. De lo que hablamos es que en ningún caso vamos a comenzar a utilizar la vacuna sin demostrar su real eficacia”, dijo.
“Eficacia ante la enfermedad hoy no existe forma de medir en término de respuesta inmune o de predecir cuál va a ser la eficacia frente al virus. Estamos hablando de que la vacuna induce respuestas inmunes diversas”, dijo.
Por lo tanto, qué sabemos hoy: “Sabemos que la aplicación de dos dosis de Soberana 02 induce una respuesta inmune potente en un porciento importante de individuos, en el término de inducción de anticuerpos neutralizantes. Induce también una importante respuesta inmune celular, no es solamente anticuerpos, sino que hay células que se despiertan y que van a contribuir a proteger a la persona de la enfermedad.
En qué medida estos dos elementos combinan frente a la enfermedad, hoy en el mundo no se sabe. Sabemos que la aplicación de una dosis de Soberana Plus sobre sujetos con dos dosis de Soberana 02 es mucho mejor que la aplicación de una tercera dosis de Soberana 02 a esos sujetos, y por lo tanto ese es un elemento que ya tenemos claro”, refirió Vérez Bencomo.
“No es una dosis de la misma vacuna, estamos hablando que esa combinación de dos dosis de Soberana 02 con una de Soberana Plus sube todavía más la respuesta inmune.
Evidentemente en la fase III tenemos que medir la eficacia de la vacuna, porque es muy posible que Soberana 02 tenga eficacia ante la cepa que está circulando hoy, pero tenemos que estar preparados para saber qué eficacia necesitaríamos para que fuera altamente eficaz ante la nueva cepa, si apareciera. Y esa información nos hace falta. La única manera de tenerla es que esos dos brazos de vacuna, cada uno se mueva independiente”, señaló el director general del IFV.
Al respecto, María Eugenia Toledo Romaní, investigadora principal del ensayo clínico fase III, del IPK, precisó que es una exigencia internacional no solo demostrar eficacia directamente en aquella población que usted vacuna, sino cuál es el efecto, cuando ya tiene altas coberturas de vacunación, en la remisión de la enfermedad.
¿Es suficiente un fase III para un registro final?
Sobre si este ensayo fase III incluirá los acuerdos de cooperación con algunos países del mundo, el doctor Vérez Bencomo precisó que si se tiene en cuenta cómo se han realizado los ensayos en las vacunas que ya se están utilizando, puede verse que un fase III no es suficiente para un registro final. “Se han dado registros condicionados a partir de un ensayo Fase III. Estamos hablando de que en el caso de la COVID-19 hay escenarios cambiantes en términos de incidencia de la enfermedad. Realmente hoy la apuesta a un ensayo de eficacia como el que estamos diseñando, se basa en la incidencia actual del virus en La Habana. Pero esta puede cambiar durante el ensayo, por lo tanto uno hace un diseño para la misma, pero se necesita tener otros ensayos Fase III que se muevan en otros escenarios con otras tasas de incidencia”.
“De ahí que estamos moviéndonos para hacer ensayos fase III de eficacia en países con los cuales tenemos acuerdos. Hay algunos que están más avanzados, otros menos, pero evidentemente también vamos a movernos a hacer ensayos de eficacia a otros lugares, pero son ensayos separados. Estamos hablando de que iniciamos nuestro ensayo de eficacia, y además de eso, estamos a las puertas de llegar a acuerdos para hacer ensayos de eficacia en otros lugares del mundo, con otras tasas de incidencia”, argumentó .
¿Cómo Cuba producirá los millones de dosis necesarios para los cubanos?
Ing. Eduardo Ojito Magaz, director general del Centro de Inmunología Molecular. Foto: Irene Pérez/ Cubadebate.
Respecto a la capacidad productiva asociada al proceso, Eduardo Ojito Magaz, director general del Centro de Inmunología Molecular (CIM) precisó que todo el producto necesario asociado a la fase III de este ensayo ya fue fabricado y liberado.
“Los estudios futuros de los nuevos ensayos clínicos, y el proceso ya de vacunación masiva necesita escalas superiores. En ese sentido, el CIM y el Instituto Finlay nos estamos preparando para introducir entre un millón y dos millones mensuales de dosis y eso nos debe permitir estar vacunando al país dentro de seis meses aproximadamente. Para ello necesitamos un aproximado de 30 millones de dosis, teniendo en cuenta que la población cubana es de 11 millones y uno de los esquemas de vacunación es de 3 dosis. Si lo dividimos entre dos, ya que estamos hablando de dos sistemas capaces de producir en grandes cantidades, podríamos decir que entre 15 y 20 millones de dosis podrían ser producidas por cada sistema. Por lo que podemos decir que ambos sistemas pueden tener la capacidad de asumir la vacunación masiva en un corto periodo de tiempo.
En caso de que tuviéramos la necesidad de montar capacidades productivas, para asumir por ejemplo, los ensayos clínicos mutinacionales en el exterior, tenemos que pensar ya en subir la escala productiva. Para ello estamos intentando montar un sistema que suba a entre 5 y 10 millones de dosis mensuales. Hoy no tenemos ningún contrato firmado, pero tenemos que tener el sistema preparado para poder afrontarlo en caso de que sea posible”, sostuvo Ojito Magaz.
Sortear obstáculos sin ceder en el máximo estándar

Conferencia de prensa de BioCubaFarma e Instituto Finlay sobre inicio del ensayo clínico fase III del candidato vacunal Soberana 02. Foto: Irene Pérez/ Cubadebate.
Han sido muchas las dificultades a sortear para pasar a la fase III y a la escalada productiva, sostuvo Yury Valdés Balbín, director adjunto del IFV. “Existe primero la situación económica del contexto país, el segundo elemento es el acceso a los recursos, a partir de proveedores que ante determinadas presiones ceden y deciden no mantener la relación con Cuba”.
“Es importante decir que el acceder o no a los insumos no es una justificación para ceder en el estándar de los que estamos haciendo. Nosotros tenemos que mantener un máximo estándar, porque estamos hablando de un medicamento que es preventivo, que va a ser destinado a población sana, y estos son precisamente los fármacos de más alto estándar regulatorio. Se está haciendo una acción de salud en alguien que en un principio no la necesita. Por tanto, el estándar de la entidad regulatoria y de la industria es muy elevado y tiene que tener los recursos necesarios y que cumplan con estos requerimientos”, sostuvo.
Para el especialista, “lo que sí podemos decir es que ha hecho organizativamente todo el esfuerzo. Hemos recibido la prioridad de la máxima dirección del país y hemos tenido, en el momento oportuno, los elementos mínimos imprescindibles. También debo decir que en determinado momento nos hemos visto impedidos, incluso, de avanzar más rápido al no poder cumplir un estándar regulatorio, por no tener el acceso a un producto.
Nosotros tenemos un lema en el proyecto que es que la unidad de tiempo en el contexto COVID es el día (en la ciencia es el año), porque en un día hay casos, hay muertos. Entonces nosotros todo lo hacemos por días y hemos estado 15-20 días impedidos de avanzar en una parte importante del proyecto, porque estamos esperando por un reactivo o un insumo necesario para cumplir el estándar regulatorio. Igual es importante acotar que hemos tenido que esperar, en la mayoría de los casos, por un bloqueo que existe y que todos ya conocen sus efectos”, apuntó.
Sin embargo, tenemos que decir que hoy estamos contando con los recursos necesarios para poder garantizar lo que queda de etapa de desarrollo del proyecto y, además de eso, poder garantizar la vacunación de los cubanos, que es el gran objetivo de todo esto, afirmó.
Por su parte, Maida Mauri Pérez, vicepresidenta primera de BioCubaFarma, hizo referencia al impacto que está teniendo el recrudecimiento del bloqueo a Cuba en este proyecto, “que en esencia es tan humanitario, no solo para la población cubana sino para el resto del mundo que, en su momento, podrá beneficiarse de las vacunas de las cuales dispondrá nuestro país”.
“Realmente el cerco financiero lo vivimos todos los días. Es una situación agobiante que impacta de manera directa en la decisión de empresarios de trabajar con nosotros en temas de codesarrollo, en la propia realización de ensayos clínicos en esos países, en la posibilidad de producir estas vacunas en otros territorios, en la capacidad que tienen muchos inversionistas en el mundo de anticipar recursos financieros para que Cuba pueda incrementar sus capacidades productivas y que muchos millones de vacunas puedan llegar a otros rincones del planeta. Hay muchos proveedores que sienten la presión y hacen efectivas las medidas que tienen en cuenta sobre ellos para el suministro de materias primas, de equipamientos que son vitales para poder desarrollar estas producciones”, señaló.
“Queremos condenar una vez más esta situación que ocurre y llamar una vez más a la comunidad internacional a combatir este injusto bloqueo, que va dirigido a temas tan sensibles como la posibilidad de que el mundo pueda disponer de manera más rápida de candidatos vacunales que estarán a disposición de la población cubana y del mundo”, afirmó.
¿Es Soberana 01A un quinto candidato vacunal?

Dra. Dagmar García Rivero, directora de investigaciones del Instituto Finlay de Vacunas. Foto: Irene Pérez/ Cubadebate.
Dagmar García Rivero, directora de Investigaciones del Instituto Finlay de Vacunas (IFV), destacó que como parte del desarrollo de Soberana 01 se han manejado varias formulaciones. “Hemos tratado de encontrar la mejor combinación entre el antígeno vacunal, el RBD dominio de unión de receptor de la proteína espiga del virus, con diferentes proporciones de la vesícula de membrana externa, que es el adyuvante que estamos usando en esa formulación. Dentro de esa formulación una de ellas tenía el RBD sin la presencia del adyuvante, y esa es la formulación que le hemos llamado Soberana 01A”, dijo.
“La propiedad distintiva de esa formulación que hemos encontrado es que tienen la capacidad de reactivar una respuesta inmune preexistente, ya sea en un individuo que estuvo expuesto al virus, dígase un convaleciente, o en individuos que hayan tenido un esquema de primo vacunación con otro candidato vacunal. O sea lo hemos demostrado en individuos convalecientes, en un ensayo clínico Fase I que hicimos y que publicamos ayer. Ahí pudimos demostrar que se produce una importante respuesta neutralizante después de una sola dosis de este candidato vacunal; y ese mismo candidato vacunal es el que estamos utilizando en el ensayo fase I y Fase II y ahora en uno de los esquemas que va al ensayo clínico Fase III como dosis de refuerzo de Soberana 02. O sea, con la lógica de que es un candidato vacunal que puede bustear o reforzar una respuesta inmune preexistente, por la vacunación o por la previa exposición al virus”, detalló.
Técnicamente sí es otro candidato vacunal, aseguró la experta. “Nosotros dentro del ensayo clínico, en un momento lo manejamos como una formulación de Soberana 01, pero en le momento en que estamos hoy, desde el punto de vista de composición, técnico, y ante la entidad regulatoria nacional, es otro producto, porque la composición no es exactamente la misma de Soberana 01”.
¿Como la aparición de nuevas cepas de coronavirus podrían afectar a la vacuna cubana?

Dr. Vicente Vérez Bencomo, director general del Instituto Finlay de Vacunas. Foto: Irene Pérez/ Cubadebate.
Vicente Vérez Bencomo, Director General del Instituto Finlay de Vacunas (IFV) corroboró que en efecto ya el IFV cuenta con este quinto candidato vacunal: Soberana 01A.
“Podemos darle la primicia que se va a llamar Soberana Plus. Soberana Plus es un concepto, y les adelanto que el preprint que acaba de salir es el primer ensayo clínico en convalecientes que se hace con una vacuna Covid a nivel mundial. No tenemos noticias de que se haya hecho un ensayo clínico en convalecientes. Se ha aplicado la vacuna, y en las personas que se ha aplicado ha coincidido que algunos son convalecientes. Se ha estudiado qué ha pasado cuando se aplica la vacuna a esta población, pero nosotros decidimos diseñar un ensayo clínico con este grupo, porque la principal amenaza que tienen son el riesgo ante las nuevas cepas”, agregó.
De acuerdo con el experto, “la inmunidad contra la cepa original pierde fuerza, especialmente contra algunas mutaciones como las que tienen ácido 484. Estamos hablando de la mutación reportada por primera vez en Sudáfrica, la reportada por primera vez en Brasil y de la evolución de la mutación original en Inglaterra. Esta mutación reduce el poder neutralizante de los anticuerpos que se inducen por la inmunidad natural, y el objetivo de nuestro ensayo con el paciente convaleciente es que tenemos que protegerlo, en primer lugar, de que se reinfeste con las nuevas cepas”, explicó.
“Eso fue lo que logramos demostrar en este ensayo clínico en convalecientes, con 30 voluntarios, y por eso pensamos que era valioso comunicarlo a la comunidad científica mundial. Es muy importante tener ese concepto en medio de la atención al convaleciente, seguir las enfermedades de este tipo de paciente y lograr que no se vuelva a reinfestar”, agregó.
Pero, ¿por qué Soberana Plus? Explicó Vérez Bencomo que cuando existe una respuesta inmune, ya sea de manera natural o por vacunas, se ha podido observar que “con este candidato seleccionamos y estimulamos solamente la respuesta contra la COVID-19 y no contra otros elementos que han estado en la pandemia. Pensamos que este candidato por su seguridad muy elevada en el convaleciente, aspecto que no ha ocurrido con otras vacunas, donde los efectos adversos en este grupo son elevados, tiene una ventaja importante”.
Al respecto, refirió que “este candidato es un elemento esencial, incluso para las propias vacunas, pues cuando en el mundo se extienda la vacunación, pasen varios meses y haya que reforzarle la inmunidad a esas personas, hay vacunas, como las que están siendo desarrolladas hoy, que no van a poder utilizarse para reforzar la inmunidad, en tanto su propio concepto no se los permite, e incluso algunas que sí se pueden utilizar pero han mostrados efectos adversos en los convalecientes”.
Un segundo elemento a tener en cuenta, dijo, es que en los ensayos clínicos de eficacia a realizar en Cuba y en diferentes partes del mundo, “vamos a medir la eficacia contra las nuevas cepas también, y tenemos la esperanza que con el diseño de esta vacuna, la eficacia contra las mismas no baje tanto”.
Como tercer elemento destacó que se trabaja aceleradamente en obtener la proteína recombinante de esta nueva combinación de mutaciones, para poder montarla en el concepto de Soberana Plus. “Pudiera ser que hubiera una Soberana Plus que tuviera la proteína recombinante de las nuevas cepas y que sirviera de refuerzo. Esa es la estrategia global que tenemos con respecto a las nuevas cepas, y creemos que combinando los tres aspectos pueda ser muy efectiva”, aseguró.
Gestión integrada para avanzar aceleradamente
A juicio de Valdés Balbín, la posibilidad de poder avanzar de manera acelerada en el contexto de la COVID-19 depende mucho de las capacidades que tengan creadas los países. “En este caso Cuba tiene una larga trayectoria y experiencia en el desarrollo de vacunas y de manejo de ensayos clínicos, y nosotros hemos logrado establecer un mecanismo de gestión de ensayo clínico con estos procesos que no empiezan con esta fase III. Desde el surgimiento de este candidato vacunal hay un mecanismo de concepción integrada de todos los ensayos clínicos, a partir de una gestión por procesos”, subrayo.
“Nosotros no estamos creando una organización nueva, estamos dándole continuidad a una organización que ya existía, que lo que empieza es a manejar ensayos clínicos más complejos cuidando rigurosamente el estándar ético, de calidad, el cumplimiento de buenas prácticas, y es eso lo que nos da la posibilidad de garantizar que vamos a tener una inclusión de más de 44 000 sujetos en un periodo de tiempo relativamente corto. Por tanto, aspiramos a que nuestro ensayo avance de manera acelerada a partir de la organización que estamos haciendo y del manejo integrado por procesos que tenemos concebido”.

Conferencia de prensa de BioCubaFarma e Instituto Finlay sobre inicio del ensayo clínico fase III del candidato vacunal Soberana 02. Foto: Irene Pérez/ Cubadebate.
Maida Mauri Pérez, vicepresidenta primera de BioCubaFarma, informó que el Centro de Ingeniería Genética y Biotecnología ya presentó el dossier de Abdala a la autoridad reguladora nacional cubana. “Esperamos que en los próximos días este candidato vacunal pueda contar con la autorización para iniciar el ensayo clínico Fase III en nuestro país”.
Soberana 02 realizará el ensayo clínico fase III en la provincia de La Habana, en ocho de sus municipios, y en el caso de Abdala se realizará en las provincias orientales Santiago de Cuba y Guantánamo.
“Le pedimos a nuestra población que, como siempre ha hecho, ayude al desarrollo de estos ensayos clínicos con mucha disciplina y con el cumplimiento riguroso del protocolo clínico que ha sido aprobado por nuestra autoridad reguladora nacional. Esta es la mejor forma que tiene nuestra población de ayudar a nuestros científicos, y a que este gran esfuerzo que está haciendo el gobierno y nuestras instituciones, para que Cuba tenga su soberanía en cuanto a la vacunación de su población, sea una feliz realidad”, sostuvo Mauri Pérez.
“Es increíble que un país pequeño como Cuba, una isla pobre en recursos materiales, pero muy rica en recursos humanos, haya llegado hasta este punto y a veces nos preguntan cómo ha sido posible esto; haciendo además buena ciencia”, reflexionó Vérez Bencomo .
Recuerdo una frase del Che cuando decía que una revolución como la nuestra es en primer lugar una obra de amor, una obra de amor al prójimo. Lo que nos sobra de recursos materiales nos sobra de amor, y esa combinación es la que ha hecho posible llevar a cabo esta hazaña, consideró.




Deja una respuesta